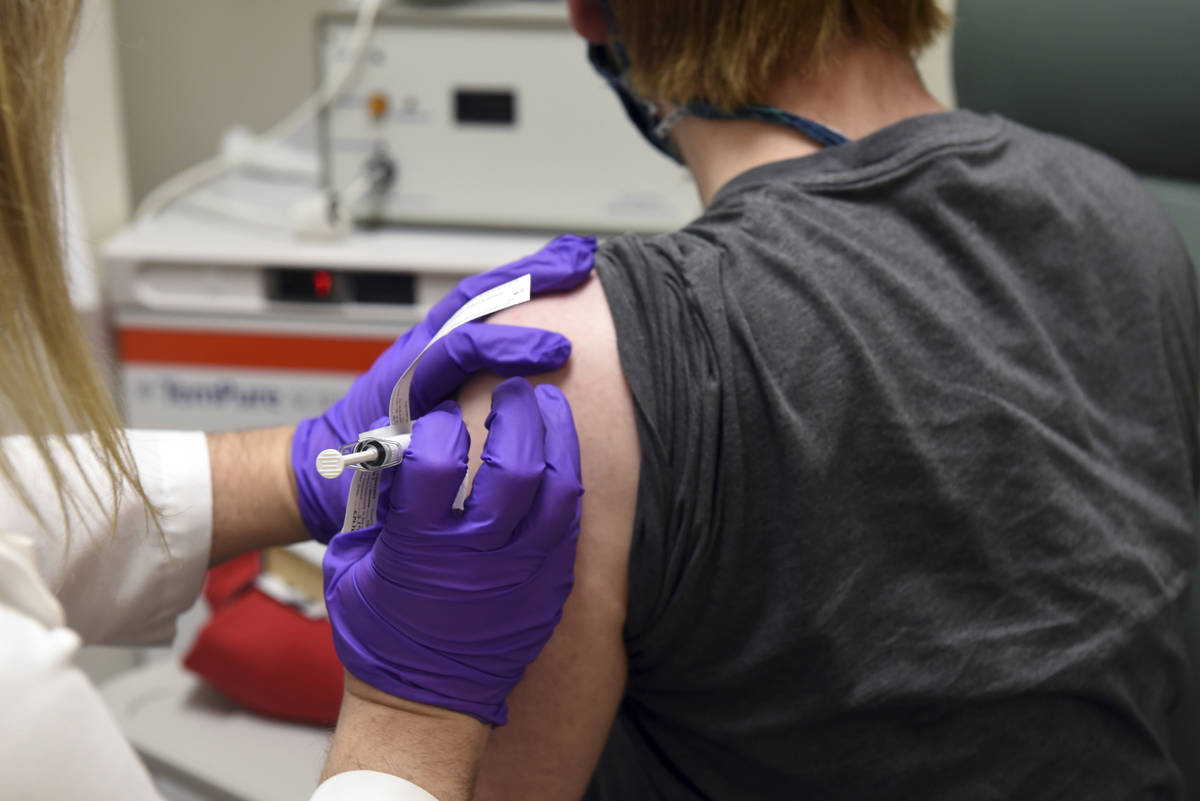
Vacuna de COVID-19 95% efectiva, Pfizer busca autorización en días
Pfizer afirma que los resultados provisionales de su estudio sobre la vacuna contra el coronavirus sugieren que las inyecciones tienen una eficacia del 95 por ciento y que la vacuna protege a las personas mayores que corren más riesgo de morir a causa de COVID-19.
El anuncio del miércoles de Pfizer y su socio alemán BioNTech (sólo una semana después de revelar los primeros resultados preliminares prometedores) llega mientras el equipo se prepara en pocos días para pedir formalmente a los reguladores de Estados Unidos que permitan el uso de emergencia de la vacuna.
También han comenzado a “rodar presentaciones” para la vacuna con los reguladores en Europa, Reino Unido y Canadá y pronto añadirán estos nuevos datos.
Pfizer y BioNTech habían estimado inicialmente que la vacuna tenía una eficacia superior al 90 por ciento después de que se hubieran contabilizado 94 infecciones en un estudio que incluyó a 44 mil personas. Con el nuevo anuncio, la compañía ha acumulado ahora 170 infecciones en el estudio, e indicó que sólo ocho de ellas ocurrieron en voluntarios que recibieron la vacuna real en lugar de una inyección ficticia. Uno de esos ocho desarrolló una enfermedad grave, dijo la compañía.
“Esta es una protección extraordinariamente fuerte”, comentó el doctor Ugur Sahin, director ejecutivo y cofundador de BioNTech, a The Associated Press.
Datos no publicados
Las empresas aún no han publicado datos detallados sobre su estudio, y los resultados no han sido analizados por expertos independientes.
Dijeron que la vacuna tenía una eficacia de más del 94 por ciento en adultos de más de 65 años, aunque no está claro exactamente cómo se determinó eso con sólo ocho infecciones en el grupo vacunado para analizar y no se proporcionó ningún desglose de las edades de esas personas.
Pero Sahin señaló que había suficientes adultos mayores inscritos en el estudio y entre los receptores de placebo que se infectaron que confía en que “esta vacuna parece funcionar en la población de mayor riesgo”.
A principios de esta semana, Moderna, Inc. anunció que su vacuna experimental parece ser 94.5 por ciento efectiva después de un análisis provisional de su estudio de etapa tardía.
Pfizer y BioNTech también argumentan que ahora tienen los datos necesarios sobre la seguridad de la vacuna para buscar la autorización de emergencia de la Food and Drug Administration.
No hay efectos secundarios graves
Las compañías no revelaron detalles de seguridad pero agregaron que no se han reportado efectos secundarios serios de la vacuna, siendo el problema más común la fatiga después de la segunda dosis de la vacuna, que afecta a cerca del cuatro por ciento de los participantes.
El estudio ha reclutado a casi 44 mil personas en Estados Unidos y otros cinco países. El ensayo continuará recolectando datos de seguridad y eficacia sobre los voluntarios durante dos años más.
Pfizer y BioNTech dijeron que esperan producir hasta 50 millones de dosis de vacunas a nivel mundial en 2020 y hasta mil 300 millones de dosis en 2021.
Las autoridades de Estados Unidos han dicho que esperan tener unos 20 millones de dosis de vacunas de Moderna y Pfizer disponibles para su distribución a finales de diciembre. Se espera que las primeras inyecciones se ofrezcan a grupos vulnerables como los trabajadores médicos y de asilos de ancianos, y a personas con problemas de salud graves.
Nevada COVID-19 Vaccination Program Playbook for Statewide Operations by Las Vegas Review-Journal on Scribd